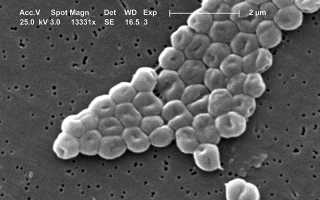
История открытия Acinetobacter ursingii
Acinetobacter ursingii был впервые описан в 1999 году, когда группа ученых из Нидерландов выделила его из образцов, полученных от пациентов с инфекциями. Это открытие стало важным шагом в понимании разнообразия рода Acinetobacter, который включает в себя множество видов, некоторые из которых являются патогенными для человека. Исходно Acinetobacter ursingii был идентифицирован как часть нормальной микрофлоры кожи и слизистых оболочек, что подчеркивает его потенциальную роль в инфекционных процессах, особенно у пациентов с ослабленным иммунитетом.
С тех пор Acinetobacter ursingii стал объектом многочисленных исследований, направленных на изучение его биологических свойств, механизмов патогенности и устойчивости к антибиотикам. Ученые начали осознавать, что этот микроорганизм может вызывать серьезные инфекции, включая пневмонию, сепсис и инфекции мочевыводящих путей. Важность Acinetobacter ursingii в клинической микробиологии продолжает расти, особенно в свете увеличения случаев инфекций, вызванных многорезистентными штаммами.
С каждым годом увеличивается количество публикаций, посвященных Acinetobacter ursingii, что свидетельствует о его значимости в области инфекционных заболеваний. Исследования показывают, что данный микроорганизм может быть не только причиной инфекций, но и потенциальным маркером для оценки состояния здоровья пациентов, особенно в условиях стационаров. Таким образом, история открытия Acinetobacter ursingii отражает не только его микробиологические характеристики, но и важность дальнейшего изучения его роли в патологии человека.
Acinetobacter ursingii — это грамотрицательная бактерия, которая привлекает внимание медицинского сообщества из-за своей устойчивости к антибиотикам и способности вызывать инфекции у людей с ослабленной иммунной системой. Врачи подчеркивают, что данная бактерия часто встречается в больничной среде и может быть источником серьезных инфекций, включая пневмонию и инфекции мочевыводящих путей. Из-за своей резистентности к множеству антибиотиков, лечение инфекций, вызванных Acinetobacter ursingii, представляет собой значительную проблему. Специалисты рекомендуют медицинским работникам повышать осведомленность о данной бактерии и внедрять строгие меры инфекционного контроля, чтобы предотвратить ее распространение. Понимание особенностей Acinetobacter ursingii важно для разработки эффективных стратегий лечения и профилактики, что в конечном итоге может спасти жизни пациентов.

Где обитает Acinetobacter ursingii?
Acinetobacter ursingii обитает в различных экологических нишах, что делает его распространенным микроорганизмом в окружающей среде. Он был выделен из различных источников, включая почву, воду и даже воздух. Эти бактерии часто обнаруживаются в больничной среде, где они могут находиться на поверхностях, медицинских инструментах и в системах вентиляции.
Основные источники Acinetobacter ursingii включают:
-
Медицинские учреждения: Бактерия часто изолируется из клинических образцов, особенно в отделениях интенсивной терапии и хирургических отделениях. Здесь она может выживать на различных поверхностях и в оборудовании, что способствует ее распространению среди пациентов.
-
Животные: Acinetobacter ursingii также может быть найден у домашних и диких животных, что указывает на возможность зоонозного переноса. Исследования показывают, что некоторые виды животных могут быть носителями этих бактерий без проявления симптомов.
-
Окружающая среда: Этот микроорганизм был выделен из почвы и сточных вод, что подчеркивает его устойчивость к неблагоприятным условиям. Acinetobacter ursingii может выживать в различных условиях, включая высокую влажность и наличие загрязняющих веществ.
Таким образом, Acinetobacter ursingii представляет собой универсальный микроорганизм, который может обитать в самых разных средах, что делает его важным объектом для изучения в контексте инфекционных заболеваний и устойчивости к антибиотикам.
Основные источники Acinetobacter ursingii
Acinetobacter ursingii в основном обитает в окружающей среде, включая почву и воду, что делает его доступным для различных источников инфекции. Однако его наиболее распространенные источники связаны с медицинскими учреждениями, где он может находиться на коже и в дыхательных путях пациентов. Этот микроорганизм часто выделяется из образцов, взятых у пациентов с инфекциями, а также из окружающих предметов и оборудования, таких как катетеры, хирургические инструменты и другие медицинские устройства.
Кроме того, Acinetobacter ursingii может быть обнаружен на руках медицинского персонала, что подчеркивает важность соблюдения правил гигиены и дезинфекции в лечебных учреждениях. Исследования показывают, что этот микроорганизм может выживать на различных поверхностях в течение длительного времени, что способствует его распространению и увеличивает риск инфекций, особенно в отделениях интенсивной терапии и среди пациентов с ослабленным иммунитетом.
Также стоит отметить, что Acinetobacter ursingii может быть частью нормальной микрофлоры человека, что делает его присутствие в организме менее заметным. Однако при определенных условиях, таких как хирургические вмешательства, длительная госпитализация или наличие хронических заболеваний, этот микроорганизм может стать патогенным и вызвать серьезные инфекции.
Acinetobacter ursingii — это бактерия, которая привлекает внимание ученых и медиков из-за своей устойчивости к антибиотикам и способности вызывать инфекции у людей с ослабленным иммунитетом. Многие специалисты подчеркивают важность изучения этой бактерии, так как она может быть причиной серьезных заболеваний, особенно в больничной среде. Люди, работающие в здравоохранении, отмечают, что Acinetobacter ursingii часто встречается у пациентов с хроническими заболеваниями или после хирургических вмешательств. Знание о ее характеристиках и путях передачи может помочь в разработке эффективных методов профилактики и лечения. Кроме того, осведомленность о данной бактерии важна для общественного здоровья, так как она может стать угрозой в условиях увеличения антибиотикорезистентности.

Как Acinetobacter ursingii вызывает заболевания?
Acinetobacter ursingii является важным патогеном, способным вызывать различные инфекции у человека. Этот микроорганизм чаще всего ассоциируется с инфекциями у пациентов с ослабленным иммунитетом, таких как больные в стационарах, особенно в отделениях интенсивной терапии. Понимание механизмов, с помощью которых Acinetobacter ursingii вызывает заболевания, имеет решающее значение для разработки эффективных методов лечения и профилактики.
Типы инфекций, вызываемых Acinetobacter ursingii, включают пневмонию, инфекции мочевыводящих путей, раневые инфекции и сепсис. Эти инфекции могут развиваться как у пациентов с предрасполагающими факторами, такими как наличие хронических заболеваний, так и у здоровых людей в условиях неблагоприятной окружающей среды, например, в медицинских учреждениях. Пневмония, вызванная Acinetobacter ursingii, часто наблюдается у пациентов, находящихся на механической вентиляции, где микроорганизм может проникать в легкие через интубационные трубки. Инфекции мочевыводящих путей могут возникать в результате катетеризации, а раневые инфекции — в результате хирургических вмешательств или травм.
Механизмы патогенности Acinetobacter ursingii разнообразны и включают несколько ключевых аспектов. Во-первых, адгезия к клеткам хозяина играет важную роль в колонизации и установлении инфекции. Микроб способен прикрепляться к эпителиальным клеткам, что позволяет ему избегать механизмов защиты организма и создавать условия для размножения.
Во-вторых, выработка вирулентных факторов, таких как экзотоксины и ферменты, способствует повреждению тканей хозяина и нарушению иммунного ответа. Эти факторы могут способствовать инвазии клеток и разрушению клеточных структур, что усугубляет течение инфекции.
Наконец, Acinetobacter ursingii демонстрирует значительное сопротивление к антибиотикам, что делает лечение инфекций, вызванных этим микроорганизмом, особенно сложным. Устойчивость к множеству антибиотиков обусловлена как генетическими механизмами, так и способностью микроорганизма обмениваться генами устойчивости с другими бактериями. Это создает серьезные проблемы для клинической практики, так как стандартные схемы лечения могут оказаться неэффективными.
Таким образом, Acinetobacter ursingii представляет собой серьезную угрозу для здоровья, особенно в условиях медицинских учреждений. Понимание механизмов его патогенности и инфекционного процесса является необходимым для разработки новых стратегий диагностики, лечения и профилактики инфекций, вызванных этим микроорганизмом.
Типы инфекций, вызываемых Acinetobacter ursingii
Acinetobacter ursingii может вызывать различные типы инфекций, что делает его значимым патогеном в клинической практике. Основные типы инфекций, ассоциируемые с этим микроорганизмом, включают:
-
Инфекции дыхательных путей. Acinetobacter ursingii может стать причиной пневмонии, особенно у пациентов, находящихся на искусственной вентиляции легких. Инфекции дыхательных путей часто возникают в условиях стационара и могут приводить к тяжелым осложнениям.
-
Инфекции мочевыводящих путей. Этот микроорганизм также может вызывать инфекции мочевыводящих путей, включая цистит и пиелонефрит. Такие инфекции чаще всего наблюдаются у пациентов с катетерами или другими инвазивными устройствами.
-
Сепсис. Acinetobacter ursingii способен вызывать системные инфекции, такие как сепсис, что представляет собой серьезную угрозу для жизни, особенно у пациентов с ослабленным иммунитетом или при наличии других сопутствующих заболеваний.
-
Инфекции кожи и мягких тканей. Микроб может стать причиной инфекций кожи, включая раневые инфекции и абсцессы. Эти инфекции могут развиваться как у здоровых людей, так и у пациентов с нарушенной целостностью кожи.
-
Инфекции у пациентов с ослабленным иммунитетом. У людей с иммунодефицитом, таких как пациенты с ВИЧ, онкологическими заболеваниями или после трансплантации органов, Acinetobacter ursingii может вызывать тяжелые и трудно поддающиеся лечению инфекции.
Эти инфекции могут быть особенно опасными, так как Acinetobacter ursingii часто демонстрирует устойчивость к множеству антибиотиков, что затрудняет их лечение и требует использования альтернативных терапевтических подходов.

Механизмы патогенности Acinetobacter ursingii
Acinetobacter ursingii обладает несколькими механизмами патогенности, которые способствуют его способности вызывать инфекции. Эти механизмы позволяют микроорганизму эффективно взаимодействовать с клетками хозяина, уклоняться от иммунного ответа и выживать в неблагоприятных условиях.
Адгезия к клеткам хозяина является первым шагом в процессе инфекционного заболевания. Acinetobacter ursingii использует специальные белки и молекулы, которые позволяют ему прочно прикрепляться к клеточным мембранам. Это взаимодействие не только способствует колонизации, но и создает условия для дальнейшего размножения и распространения бактерий в организме. Эффективная адгезия также затрудняет удаление микроорганизма с помощью механических факторов, таких как потоки крови или лимфы.
Выработка вирулентных факторов — еще один ключевой аспект патогенности Acinetobacter ursingii. Эти факторы могут включать токсичные белки, ферменты и другие молекулы, которые помогают бактериям разрушать ткани хозяина и вызывать воспалительные реакции. Например, некоторые из этих вирулентных факторов могут нарушать целостность клеточных мембран, что приводит к гибели клеток и способствует распространению инфекции.
Сопротивление к антибиотикам является одной из наиболее серьезных проблем, связанных с Acinetobacter ursingii. Этот микроорганизм демонстрирует высокую степень устойчивости к различным классам антибиотиков, что затрудняет лечение инфекций. Механизмы устойчивости могут включать выработку β-лактамаз, которые разрушают антибиотики, а также изменение целевых молекул, к которым направлены антибиотики. Кроме того, Acinetobacter ursingii может образовывать биопленки, что значительно увеличивает его защиту от воздействия антибактериальных препаратов и иммунной системы хозяина.
Таким образом, понимание механизмов патогенности Acinetobacter ursingii имеет важное значение для разработки новых стратегий диагностики и лечения инфекций, вызванных этим микроорганизмом. Исследования в этой области помогут улучшить подходы к борьбе с инфекциями и снизить риск их распространения в медицинских учреждениях.
1. Адгезия к клеткам хозяина
Одним из ключевых механизмов патогенности Acinetobacter ursingii является его способность к адгезии к клеткам хозяина. Этот процесс начинается с взаимодействия микроорганизма с клеточной поверхностью, что позволяет ему закрепляться на тканях и избегать вымывания из организма. Адгезия осуществляется благодаря специфическим белкам и полисахаридам, которые находятся на поверхности бактерий. Эти молекулы взаимодействуют с рецепторами на клетках хозяина, что способствует образованию устойчивых колоний.
Кроме того, адгезия играет важную роль в формировании биопленок. Биопленки — это сложные структуры, состоящие из микроорганизмов, которые прикрепляются к поверхности и окружены экстрацеллюлярным матриксом. Они обеспечивают защиту бактерий от иммунной системы хозяина и антибиотиков, что делает инфекции, вызванные Acinetobacter ursingii, особенно трудноизлечимыми. В условиях госпиталя, где часто встречаются инвазивные процедуры, такие как установка катетеров или вентиляционных трубок, риск формирования биопленок значительно возрастает.
Исследования показывают, что адгезия Acinetobacter ursingii может зависеть от различных факторов, включая состав среды, pH и наличие определенных ионов. Это открывает новые горизонты для разработки методов, направленных на блокировку адгезии, что может стать одним из подходов к профилактике инфекций, вызванных этим микроорганизмом. Понимание механизмов адгезии также может помочь в создании новых диагностических тестов и терапевтических стратегий, направленных на борьбу с инфекциями, вызванными Acinetobacter ursingii.
2. Выработка вирулентных факторов
Acinetobacter ursingii вырабатывает ряд вирулентных факторов, которые способствуют его патогенности и способности вызывать инфекции. Эти факторы играют ключевую роль в взаимодействии микроорганизма с клетками хозяина и в механизмах, позволяющих ему избегать иммунного ответа.
Во-первых, одним из основных вирулентных факторов является способность Acinetobacter ursingii к адгезии. Микроорганизм обладает специальными белками, которые позволяют ему прочно прикрепляться к клеткам эпителия, что является первым шагом в процессе инфекционного заболевания. Эта адгезия не только способствует колонизации, но и затрудняет удаление бактерий иммунной системой.
Во-вторых, Acinetobacter ursingii вырабатывает экзотоксины, которые могут повреждать клетки хозяина и вызывать воспалительные реакции. Эти токсины могут нарушать нормальные функции клеток, что способствует развитию инфекционного процесса и усугубляет состояние пациента. Например, некоторые токсины могут вызывать апоптоз (программированную клеточную смерть) клеток иммунной системы, что снижает защитные силы организма.
Кроме того, Acinetobacter ursingii обладает способностью к образованию биопленок. Биопленки представляют собой сложные структуры, состоящие из микроорганизмов и внеклеточного матрикса, которые обеспечивают защиту бактерий от воздействия антибиотиков и иммунных клеток. Это делает инфекции, вызванные Acinetobacter ursingii, особенно трудными для лечения, так как стандартные методы терапии могут оказаться неэффективными.
Наконец, стоит отметить, что Acinetobacter ursingii также может вырабатывать ферменты, разрушающие антибиотики, такие как бета-лактамазы. Эти ферменты способны инактивировать широкий спектр антибиотиков, что приводит к устойчивости к лечению и затрудняет выбор эффективной терапии для пациентов с инфекциями, вызванными данным микроорганизмом.
Таким образом, выработка вирулентных факторов Acinetobacter ursingii играет ключевую роль в его патогенности и устойчивости к антибиотикам, что делает его серьезной угрозой для здоровья, особенно среди уязвимых групп населения.
3. Сопротивление к антибиотикам
Acinetobacter ursingii демонстрирует значительное сопротивление к различным классам антибиотиков, что делает его особенно опасным патогеном в клинической практике. Это сопротивление обусловлено несколькими факторами, включая наличие генов, ответственных за устойчивость, а также способность к горизонтальному переносу этих генов между бактериями.
Одним из основных механизмов устойчивости является выработка бета-лактамаз — ферментов, которые разрушают бета-лактамные антибиотики, такие как пенициллины и цефалоспорины. Acinetobacter ursingii может производить как классические, так и расширенные спектры бета-лактамаз, что значительно затрудняет лечение инфекций, вызванных этим микроорганизмом.
Кроме того, Acinetobacter ursingii способен изменять проницаемость своей клеточной мембраны, что препятствует проникновению антибиотиков внутрь клетки. Это достигается за счет изменения структуры пориновых белков, которые отвечают за транспорт веществ через мембрану. Изменение экспрессии этих белков может привести к снижению чувствительности к антибиотикам.
Также стоит отметить, что Acinetobacter ursingii может активно выводить антибиотики из клетки с помощью систем активного выведения, таких как RND (Resistance-Nodulation-Division) и MFS (Major Facilitator Superfamily). Эти системы позволяют бактериям эффективно избавляться от антибиотиков, которые все же смогли проникнуть внутрь.
Наконец, генетическая изменчивость этого микроорганизма способствует его способности адаптироваться к различным условиям, включая воздействие антибиотиков. Это делает Acinetobacter ursingii не только устойчивым к текущим методам лечения, но и способным развивать новые механизмы устойчивости, что представляет собой серьезную проблему для здравоохранения.
Таким образом, понимание механизмов устойчивости Acinetobacter ursingii является ключевым для разработки новых стратегий лечения и профилактики инфекций, вызванных этим патогеном.
Диагностика инфекций, вызванных Acinetobacter ursingii
Диагностика инфекций, вызванных Acinetobacter ursingii, представляет собой сложный и многоступенчатый процесс, который требует применения различных методов для точного определения наличия этого микроорганизма. Важно отметить, что Acinetobacter ursingii может быть трудно дифференцировать от других видов рода Acinetobacter, что делает диагностику еще более сложной.
Основные методы диагностики включают микробиологические, молекулярные и серологические подходы. Микробиологические методы основаны на выделении и идентификации бактерий из образцов, таких как кровь, моча или раневые выделения. Для этого образцы помещаются на специальные питательные среды, где происходит рост микроорганизмов. После этого проводятся тесты на определение биохимических свойств, которые помогают идентифицировать Acinetobacter ursingii.
Молекулярные методы, такие как полимеразная цепная реакция (ПЦР), становятся все более популярными благодаря своей высокой чувствительности и специфичности. Эти методы позволяют обнаруживать генетический материал Acinetobacter ursingii в образцах, что значительно ускоряет процесс диагностики и позволяет выявлять инфекции на ранних стадиях.
Серологические методы, хотя и менее распространены, также могут использоваться для диагностики инфекций, вызванных Acinetobacter ursingii. Они основаны на выявлении антител к этому микроорганизму в сыворотке крови пациента. Однако, из-за возможности перекрестной реакции с другими бактериями, такие методы требуют осторожности в интерпретации результатов.
Важным аспектом диагностики является также оценка клинической картины пациента и наличие факторов риска, таких как иммуносупрессия или недавние хирургические вмешательства. Это позволяет врачам более точно определить вероятность наличия инфекции, вызванной Acinetobacter ursingii, и выбрать соответствующие методы диагностики.
Таким образом, комплексный подход к диагностике инфекций, вызванных Acinetobacter ursingii, включает в себя использование различных методов, что позволяет повысить точность и своевременность выявления этого патогена.
Основные методы диагностики
Основные методы диагностики инфекций, вызванных Acinetobacter ursingii, включают как микробиологические, так и молекулярно-генетические подходы.
Первым шагом в диагностике является сбор образцов биологических жидкостей, таких как кровь, моча, мокрота или раневые выделения, в зависимости от клинической картины. Эти образцы затем подвергаются посеву на питательные среды, что позволяет изолировать и идентифицировать микроорганизмы. Для Acinetobacter ursingii характерно медленное размножение, поэтому необходимо учитывать время инкубации, которое может составлять от 24 до 48 часов.
После изоляции бактерий, их идентификация может быть выполнена с помощью различных методов, включая биохимические тесты, такие как тест на окисление и ферментацию углеводов. Однако, для более точной идентификации все чаще применяются молекулярно-генетические методы, такие как полимеразная цепная реакция (ПЦР). Этот метод позволяет обнаружить специфические гены, характерные для Acinetobacter ursingii, что значительно ускоряет процесс диагностики и повышает его точность.
Кроме того, важно провести тестирование на чувствительность к антибиотикам, поскольку Acinetobacter ursingii известен своей способностью к развитию устойчивости к различным антибактериальным препаратам. Для этого используются методы диффузии в агаре или микробные минимальные ингибирующие концентрации (МИК). Эти тесты помогают определить, какие антибиотики будут наиболее эффективными для лечения инфекции.
Таким образом, комплексный подход, включающий как традиционные микробиологические методы, так и современные молекулярные техники, позволяет эффективно диагностировать инфекции, вызванные Acinetobacter ursingii, и своевременно начать лечение.
Лечение инфекций, вызванных Acinetobacter ursingii
Лечение инфекций, вызванных Acinetobacter ursingii, представляет собой сложную задачу, учитывая его устойчивость к множеству антибиотиков и различные клинические проявления. Основные подходы к лечению включают использование комбинаций антибиотиков, тщательный мониторинг состояния пациента и применение поддерживающей терапии.
Одним из ключевых аспектов лечения является выбор антибиотиков. Из-за высокой степени устойчивости Acinetobacter ursingii к традиционным антибиотикам, таких как пенициллины и цефалоспорины, необходимо проводить антибиотикограмму для определения чувствительности микроорганизма к различным антибактериальным препаратам. В некоторых случаях могут быть эффективны карбапенемы, однако их использование должно быть ограничено из-за риска развития дальнейшей устойчивости.
Комбинированная терапия часто оказывается более эффективной, чем монотерапия. Врач может назначить сочетание антибиотиков, чтобы увеличить шансы на успешное лечение и снизить риск рецидива инфекции. Например, комбинация карбапенемов с аминогликозидами или полимиксинами может быть рассмотрена в зависимости от клинической ситуации и результатов антибиотикограммы.
Поддерживающая терапия также играет важную роль в лечении инфекций, вызванных Acinetobacter ursingii. Это может включать в себя коррекцию нарушений водно-электролитного баланса, поддержку функций органов и систем, а также использование иммуномодуляторов в случаях, когда это необходимо. Важно также обеспечить адекватный уход за пациентами с ослабленным иммунитетом, чтобы предотвратить развитие новых инфекций.
В некоторых случаях, особенно при тяжелых инфекциях, может потребоваться применение более агрессивных методов лечения, таких как хирургическое вмешательство для удаления инфицированных тканей или дренирования абсцессов. Это может значительно улучшить исход лечения и снизить риск системных осложнений.
Таким образом, лечение инфекций, вызванных Acinetobacter ursingii, требует комплексного подхода, включающего правильный выбор антибиотиков, комбинированную терапию и поддерживающие меры. Своевременная диагностика и индивидуализированный подход к каждому пациенту являются ключевыми факторами для достижения успешного результата.
Основные подходы к лечению
Лечение инфекций, вызванных Acinetobacter ursingii, представляет собой сложную задачу, учитывая его устойчивость к многим антибиотикам. Основные подходы к лечению включают использование комбинаций антибиотиков, которые могут быть более эффективными, чем монотерапия. Часто применяются карбапенемы, такие как меропенем и имипенем, которые обладают широким спектром действия и могут подавлять рост этого микроорганизма.
Однако, в связи с растущей устойчивостью Acinetobacter ursingii к карбапенемам, врачи могут рассмотреть возможность использования других классов антибиотиков, таких как полимиксины (например, колистин) или тетрациклины. Эти препараты могут быть полезны в случаях, когда стандартные схемы лечения оказываются неэффективными.
Важно также учитывать, что лечение должно быть индивидуализированным. Это означает, что выбор антибиотиков должен основываться на результатах антибиограммы, которая позволяет определить чувствительность конкретного штамма Acinetobacter ursingii к различным антибиотикам. Таким образом, врачи могут назначить наиболее эффективное лечение, минимизируя риск побочных эффектов и развития дополнительных устойчивых штаммов.
Кроме антибиотикотерапии, поддерживающая терапия также играет важную роль. Это может включать в себя поддержание адекватного уровня жидкости, электролитов и, при необходимости, использование иммуностимуляторов для повышения защитных сил организма. В случаях тяжелых инфекций может потребоваться госпитализация и интенсивная терапия.
Таким образом, подходы к лечению инфекций, вызванных Acinetobacter ursingii, требуют комплексного и многогранного подхода, который учитывает как особенности микроорганизма, так и состояние пациента.
Профилактика инфекций, вызванных Acinetobacter ursingii
Профилактика инфекций, вызванных Acinetobacter ursingii, является важной задачей в области инфекционной безопасности, особенно в медицинских учреждениях, где риск передачи этого микроорганизма значительно возрастает. Основные меры профилактики направлены на снижение вероятности заражения и распространения Acinetobacter ursingii среди пациентов и медицинского персонала.
Одной из ключевых мер является соблюдение строгих стандартов гигиены и санитарии в больницах и клиниках. Это включает регулярную дезинфекцию поверхностей, оборудования и медицинских инструментов, а также использование одноразовых материалов, когда это возможно. Медицинский персонал должен соблюдать правила мытья рук, особенно перед и после контакта с пациентами, чтобы предотвратить передачу инфекции.
Также важно проводить обучение и тренинги для медицинского персонала по вопросам инфекционного контроля и профилактики. Знание о путях передачи Acinetobacter ursingii и мерах по его предотвращению поможет снизить риск вспышек инфекций в медицинских учреждениях.
Контроль за использованием антибиотиков также играет важную роль в профилактике инфекций, вызванных Acinetobacter ursingii. Необоснованное применение антибиотиков может способствовать развитию устойчивых штаммов, что делает лечение инфекций более сложным. Поэтому необходимо следовать рекомендациям по рациональному использованию антибиотиков и проводить мониторинг их применения.
Кроме того, важно проводить эпидемиологический мониторинг и отслеживание случаев инфекций, вызванных Acinetobacter ursingii, чтобы своевременно выявлять и реагировать на вспышки. Это может включать в себя регулярные обследования пациентов и анализы на наличие этого микроорганизма, особенно в отделениях интенсивной терапии и хирургии.
В заключение, профилактика инфекций, вызванных Acinetobacter ursingii, требует комплексного подхода, включающего соблюдение гигиенических норм, обучение персонала, контроль за использованием антибиотиков и мониторинг инфекционной ситуации. Эти меры помогут снизить риск заражения и защитить здоровье пациентов и медицинского персонала.
Основные меры профилактики
Профилактика инфекций, вызванных Acinetobacter ursingii, требует комплексного подхода, направленного на снижение риска передачи и распространения этого микроорганизма, особенно в медицинских учреждениях, где пациенты наиболее уязвимы.
Одной из основных мер профилактики является соблюдение строгих стандартов гигиены и инфекционного контроля. Это включает регулярное мытье рук медицинским персоналом, использование антисептиков и соблюдение правил асептики при проведении процедур. Важно также проводить регулярные тренинги для сотрудников, чтобы они были осведомлены о рисках, связанных с Acinetobacter ursingii, и знали, как правильно реагировать на возможные случаи заражения.
Другая важная мера — это изоляция пациентов с подтвержденными инфекциями, вызванными Acinetobacter ursingii. Это помогает предотвратить дальнейшее распространение микроорганизма в больничной среде. Также следует уделять внимание дезинфекции медицинского оборудования и поверхностей, которые могут быть загрязнены, поскольку Acinetobacter ursingii может выживать на различных поверхностях в течение длительного времени.
Кроме того, необходимо контролировать использование антибиотиков в медицинских учреждениях. Избыточное и нецелевое применение антибиотиков может способствовать развитию устойчивых штаммов Acinetobacter ursingii, что затрудняет лечение инфекций. Программы антимикробной терапии должны быть внедрены для оптимизации использования антибиотиков и снижения риска возникновения устойчивости.
Наконец, важно проводить мониторинг и эпидемиологические исследования для выявления вспышек инфекций, связанных с Acinetobacter ursingii. Сбор данных о случаях заражения и анализ их причин поможет разработать более эффективные стратегии профилактики и контроля.
В целом, комплексный подход к профилактике инфекций, вызванных Acinetobacter ursingii, включает в себя соблюдение гигиенических норм, изоляцию инфицированных пациентов, контроль за использованием антибиотиков и активный мониторинг ситуации в медицинских учреждениях.
Перспективы исследований Acinetobacter ursingii
Перспективы исследований Acinetobacter ursingii открывают новые горизонты в области микробиологии и инфекционных заболеваний. Учитывая растущую значимость этого микроорганизма в клинической практике, ученые сосредоточены на нескольких ключевых направлениях.
Одним из основных направлений является изучение механизмов устойчивости Acinetobacter ursingii к антибиотикам. Понимание генетических и биохимических основ этого процесса может привести к разработке новых стратегий лечения и предотвращения распространения устойчивых штаммов. Исследования в этой области могут включать геномные и протеомные анализы, которые помогут выявить специфические гены, ответственные за устойчивость.
Также важным направлением является изучение патогенеза Acinetobacter ursingii. Ученые стремятся глубже понять, как этот микроорганизм взаимодействует с клетками хозяина, какие факторы способствуют его вирулентности и как он вызывает различные инфекции. Это знание может способствовать разработке новых вакцин и терапевтических подходов.
Кроме того, исследователи обращают внимание на экосистемы, в которых обитает Acinetobacter ursingii. Изучение его распространения в окружающей среде, а также в медицинских учреждениях может помочь в разработке эффективных мер профилактики и контроля инфекций. Это включает в себя мониторинг и анализ образцов из различных источников, таких как вода, почва и медицинские инструменты.
Наконец, перспективы исследований Acinetobacter ursingii также связаны с его ролью в микробиоме человека. Понимание взаимодействия этого микроорганизма с другими бактериями и его влияния на здоровье человека может открыть новые возможности для применения пробиотиков и других средств, направленных на восстановление нормальной микрофлоры.
Таким образом, исследования Acinetobacter ursingii имеют многообещающие перспективы, которые могут значительно повлиять на медицину и общественное здоровье в целом.
Ключевые направления будущих исследований
Ключевые направления будущих исследований Acinetobacter ursingii сосредоточены на нескольких важных аспектах, которые могут помочь в понимании его патогенности и разработке новых методов борьбы с инфекциями, вызванными этим микроорганизмом.
Во-первых, необходимо углубленное изучение механизмов адгезии Acinetobacter ursingii к клеткам хозяина. Понимание того, как этот микроорганизм прикрепляется к клеткам и тканям, может открыть новые горизонты для разработки антиадгезивных терапий, которые могут предотвратить начало инфекции.
Во-вторых, исследование вирулентных факторов, вырабатываемых Acinetobacter ursingii, является ключевым направлением. Это включает в себя анализ белков, которые способствуют выживанию и размножению бактерий в организме хозяина, а также факторов, которые помогают им избегать иммунного ответа. Эти данные могут быть использованы для создания вакцин или других иммунотерапий.
В-третьих, важным направлением является изучение механизмов устойчивости к антибиотикам. Acinetobacter ursingii уже продемонстрировал способность к развитию резистентности к множеству антибиотиков, что делает его особенно опасным патогеном. Исследования в этой области могут помочь в разработке новых антибиотиков или альтернативных методов лечения, таких как фаготерапия.
Кроме того, необходимо проводить эпидемиологические исследования, чтобы лучше понять распространение Acinetobacter ursingii в различных популяциях и условиях. Это поможет выявить группы риска и разработать стратегии для профилактики инфекций.
Наконец, важным направлением является изучение взаимодействия Acinetobacter ursingii с другими микроорганизмами в микробиоме человека. Это может дать новые идеи о том, как этот патоген влияет на здоровье человека и как можно использовать микробиом для борьбы с инфекциями.
Таким образом, будущее исследований Acinetobacter ursingii обещает быть многообещающим, с возможностью значительного вклада в понимание и лечение инфекционных заболеваний, вызванных этим микроорганизмом.
Заключение
Acinetobacter ursingii представляет собой важный объект исследований в области микробиологии и инфекционных заболеваний. Его способность вызывать инфекции у людей с ослабленным иммунитетом и устойчивость к множеству антибиотиков делают его серьезной угрозой для здоровья. Важно отметить, что понимание механизмов патогенности этого микроорганизма и его распространения может помочь в разработке более эффективных стратегий профилактики и лечения.
С учетом растущей проблемы антибиотикорезистентности, исследование Acinetobacter ursingii становится все более актуальным. Ученые продолжают изучать его генетические особенности, чтобы выявить новые мишени для терапии и улучшить диагностику инфекций. Также необходимы дальнейшие исследования для понимания экологии этого микроорганизма и его взаимодействия с другими патогенами.
В заключение, Acinetobacter ursingii — это не просто еще один микроорганизм, а серьезный вызов для медицины. Осознание его значимости и активное изучение помогут снизить риски, связанные с инфекциями, вызванными этим патогеном, и улучшить исходы лечения для пациентов.
Вопрос-ответ
Вреден ли ацинетобактер для человека?
Acinetobacter может жить на или в организме пациента, не вызывая инфекции или симптомов, но также может потенциально вызывать различные заболевания, включая инфекции легких («пневмонию») и инфекции крови, ран или мочевыводящих путей . Типичные симптомы пневмонии могут включать лихорадку, озноб или кашель.
Откуда взялся acinetobacter ursingii?
Acinetobacter — это грамотрицательный, неподвижный организм, который часто встречается в почве и воде и, как известно, колонизирует внутривенные жидкости. В целом, Acinetobacter обладает низкой вирулентностью. Однако он способен вызывать инфекцию у пациентов с ослабленным иммунитетом и нейтропенией, и становится все более устойчивым к лекарственным препаратам.
Как можно заразиться ацинетобактером?
Контакт с загрязненным оборудованием . Контакт от человека к человеку, часто через загрязненные руки.
Как лечится ацинетобактер?
Полимиксины – Полимиксины (полимиксин B и колистин [полимиксин E]) обычно используются для изолятов Acinetobacter, устойчивых к препаратам первой линии. Производные тетрациклина – Антибиотики класса тетрациклинов (например, миноциклин, доксициклин, тигециклин) часто обладают активностью против Acinetobacter [96-98].
Советы
СОВЕТ №1
Изучите информацию о Acinetobacter ursingii, чтобы понимать его роль в микробиоме человека и его потенциальные риски. Это поможет вам быть более осведомленным о возможных инфекциях и мерах предосторожности.
СОВЕТ №2
Обратите внимание на профилактические меры, такие как соблюдение гигиенических норм и вакцинация, чтобы снизить риск заражения инфекциями, вызванными Acinetobacter ursingii и другими патогенами.
СОВЕТ №3
Если вы работаете в медицинской сфере или ухаживаете за больными, ознакомьтесь с протоколами инфекционного контроля, чтобы эффективно предотвращать распространение Acinetobacter ursingii в медицинских учреждениях.
СОВЕТ №4
Следите за новыми исследованиями и публикациями о Acinetobacter ursingii, так как наука о микробах постоянно развивается, и новые данные могут помочь лучше понять его поведение и влияние на здоровье человека.